Mitochondria to małe struktury znajdujące się w niemal każdej komórce naszego ciała i bardzo często nazywa się je elektrowniami komórkowymi, ponieważ to właśnie w nich powstaje większość energii potrzebnej do życia, oddychania, ruchu, pracy mózgu oraz regeneracji tkanek. Gdy mitochondria działają sprawnie, czujemy się pełni energii, szybciej się regenerujemy i lepiej tolerujemy wysiłek fizyczny oraz psychiczny, natomiast kiedy zaczynają funkcjonować gorzej, pojawia się przewlekłe zmęczenie, spadek wydolności, problemy z koncentracją, a czasem również większa podatność na choroby metaboliczne. Właśnie z tego powodu w ostatnich latach coraz częściej mówi się o czymś, co potocznie określa się mianem resetu mitochondrialnego, czyli próbie przywrócenia komórkom bardziej efektywnego wytwarzania energii oraz ograniczenia nadmiernego stresu oksydacyjnego.
Sam termin reset mitochondrialny nie jest pojęciem medycznym w ścisłym znaczeniu, lecz raczej uproszczonym określeniem stosowanym w środowiskach zajmujących się medycyną funkcjonalną, sportem wyczynowym oraz biohackingiem, gdzie opisuje się nim działania mające na celu poprawę jakości pracy mitochondriów poprzez odpowiednią dietę, sen, aktywność fizyczną, a niekiedy także zastosowanie wybranych peptydów. Aby zrozumieć, czy i kiedy takie podejście może mieć sens, warto najpierw zrozumieć, jak w ogóle dochodzi do pogorszenia funkcji mitochondriów oraz jakie mechanizmy można próbować wspierać.
Mitochondria produkują energię w procesie zwanym fosforylacją oksydacyjną, w którym wykorzystywany jest tlen, a efektem końcowym jest cząsteczka ATP, czyli podstawowe paliwo dla komórek. Proces ten jest niezwykle wydajny, lecz jednocześnie generuje reaktywne formy tlenu, które w nadmiarze mogą uszkadzać białka, lipidy oraz materiał genetyczny komórki. Jeśli stres oksydacyjny utrzymuje się długo, mitochondria zaczynają pracować mniej efektywnie, a komórka może wchodzić w stan przewlekłego zmęczenia metabolicznego. Organizm posiada naturalne mechanizmy naprawcze, takie jak autofagia i mitofagia, które pozwalają usuwać uszkodzone mitochondria i tworzyć nowe, jednak z wiekiem oraz pod wpływem przewlekłego stresu mechanizmy te mogą działać słabiej.
W kontekście resetu mitochondrialnego mówi się więc o wspieraniu procesów biogenezy mitochondriów, czyli tworzenia nowych, sprawnych struktur energetycznych, o ograniczaniu nadmiernego stanu zapalnego oraz o poprawie wrażliwości metabolicznej komórek. Właśnie w tym miejscu pojawia się temat peptydów, które są krótkimi łańcuchami aminokwasów pełniącymi funkcję sygnałową i które w niektórych przypadkach mogą wpływać na procesy regeneracyjne oraz metaboliczne.
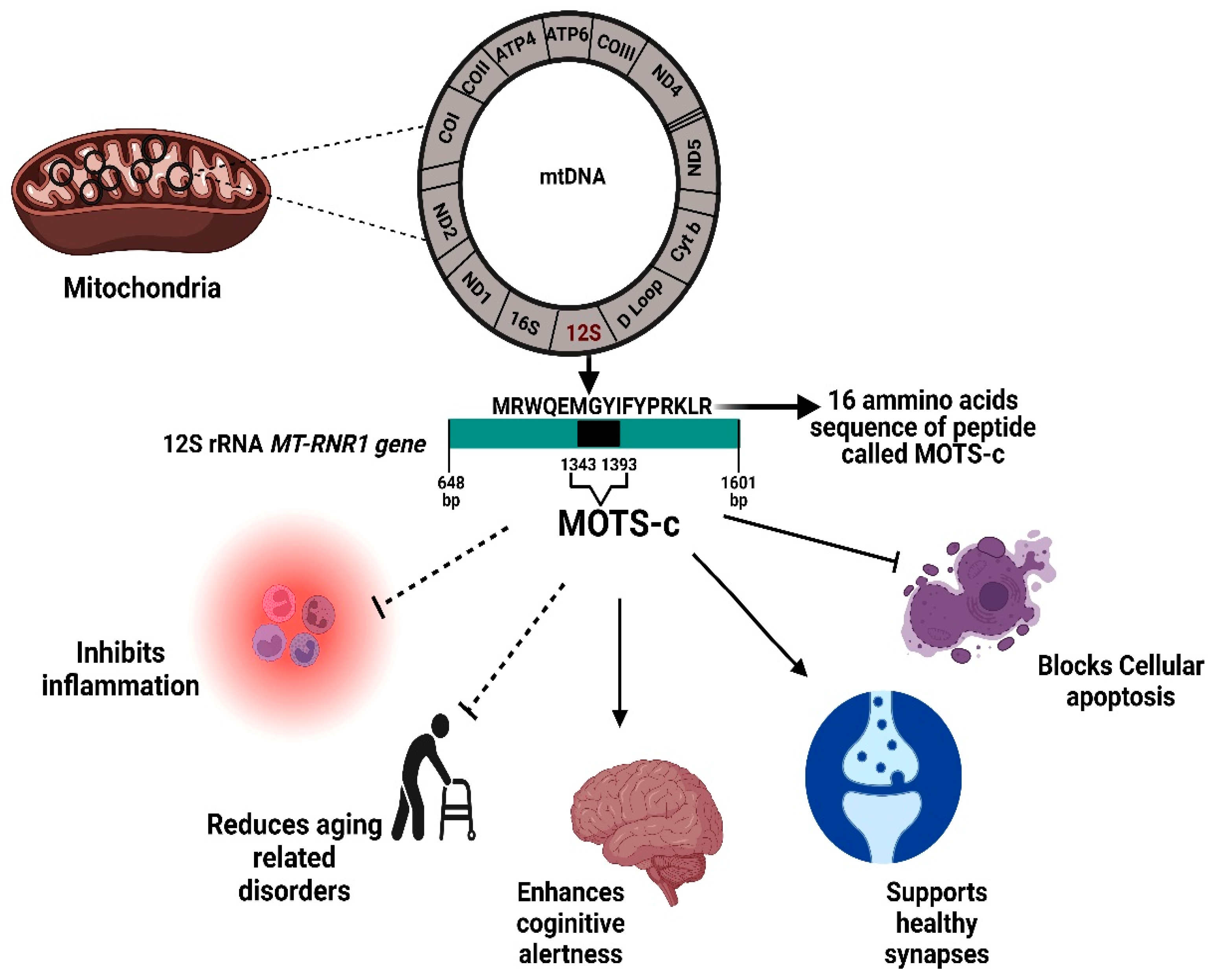
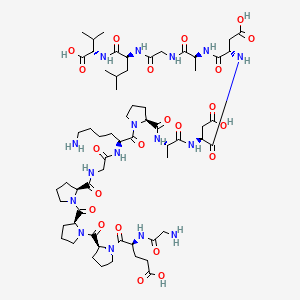
Jednym z najczęściej wymienianych w tym kontekście związków jest tak zwany MOTS-c, który jest peptydem pochodzącym bezpośrednio z DNA mitochondrialnego, co czyni go szczególnie interesującym w kontekście metabolizmu energetycznego.

4
MOTS-c, klasyfikowany jako peptyd mitochondrialny, według badań eksperymentalnych wpływa na gospodarkę glukozową oraz wrażliwość insulinową, a także może aktywować szlaki związane z AMPK, czyli enzymem uznawanym za jeden z głównych regulatorów energetycznych komórki. W praktyce oznacza to, że komórki mogą efektywniej wykorzystywać glukozę oraz kwasy tłuszczowe, co sprzyja poprawie wydolności metabolicznej, jednak należy podkreślić, że większość danych pochodzi z badań przedklinicznych, a zastosowanie kliniczne pozostaje ograniczone. MOTS-c bywa rozważany w sytuacjach, w których dominują objawy zespołu metabolicznego, przewlekłego zmęczenia związanego z zaburzeniami gospodarki energetycznej oraz w kontekście wsparcia adaptacji do wysiłku fizycznego.
Innym związkiem omawianym przy okazji resetu mitochondrialnego jest SS-31, znany również jako elamipretide, który wykazuje zdolność do oddziaływania na błonę wewnętrzną mitochondrium.


4
Elamipretide, czyli SS-31, jest peptydem zaprojektowanym tak, aby stabilizować kardiolipinę, która jest kluczowym składnikiem błony mitochondrialnej i odgrywa istotną rolę w funkcjonowaniu łańcucha oddechowego. W badaniach analizowano jego potencjał w chorobach serca oraz schorzeniach mięśniowych, gdzie uszkodzenie mitochondriów ma znaczenie patofizjologiczne. Teoretycznie mógłby on wspierać poprawę wydajności energetycznej w komórkach dotkniętych stresem oksydacyjnym, jednak również w tym przypadku nie mówimy o powszechnie dostępnej i rutynowej terapii, lecz o substancji badawczej.
W dyskusjach o resecie mitochondrialnym pojawia się również temat peptydów, które nie działają bezpośrednio na mitochondria, ale pośrednio wspierają ich funkcjonowanie poprzez poprawę regeneracji tkanek oraz redukcję stanu zapalnego. Przykładem może być BPC-157, czyli syntetyczny peptyd wywodzący się z białka żołądkowego.


4
BPC-157 opisywany jest jako związek wspierający gojenie tkanek, angiogenezę oraz regenerację, a choć nie jest klasycznym peptydem mitochondrialnym, to poprzez poprawę mikrokrążenia oraz redukcję lokalnego stanu zapalnego może pośrednio sprzyjać lepszym warunkom pracy mitochondriów. W sytuacjach, w których dominują przewlekłe mikrourazy, przeciążenia sportowe lub uszkodzenia tkanek, wsparcie regeneracji może mieć znaczenie dla ogólnej poprawy wydolności komórkowej.
Część osób interesujących się resetem mitochondrialnym zwraca również uwagę na analogi peptydów wpływających na hormon wzrostu, takie jak CJC-1295 czy ipamorelina, ponieważ hormon wzrostu oraz IGF-1 odgrywają rolę w regeneracji i biogenezie komórkowej. Jednak w tym przypadku należy być ostrożnym, gdyż ingerencja w oś hormonalną jest znacznie poważniejsza niż modulacja lokalnych mechanizmów metabolicznych, a potencjalne korzyści muszą być zawsze rozważane w kontekście możliwego wpływu na gospodarkę glukozową, lipidową oraz proliferację komórek.
Kluczowym pytaniem pozostaje jednak nie tylko jakie peptydy wybrać, lecz przede wszystkim kiedy w ogóle rozważać takie podejście. Reset mitochondrialny ma największy sens jako koncepcja wspierająca w sytuacjach, w których występują objawy przewlekłego zmęczenia metabolicznego, spadku wydolności bez jasnej przyczyny, trudności w regeneracji po wysiłku oraz cechy insulinooporności lub zespołu metabolicznego. Zanim jednak ktokolwiek zacznie rozważać jakiekolwiek peptydy, powinien zadbać o podstawy, ponieważ bez nich żaden związek nie przyniesie trwałej poprawy.
Podstawą poprawy funkcji mitochondriów jest regularna aktywność fizyczna, zwłaszcza trening interwałowy oraz siłowy, które naturalnie stymulują biogenezę mitochondrialną poprzez aktywację AMPK oraz PGC-1α. Równie ważny jest sen, ponieważ w jego trakcie zachodzą procesy naprawcze i usuwanie uszkodzonych struktur komórkowych. Dieta bogata w białko, zdrowe tłuszcze oraz mikroelementy, takie jak magnez czy koenzym Q10, stanowi fundament, bez którego trudno mówić o realnym resecie metabolicznym.
Peptydy, jeśli w ogóle są rozważane, powinny być traktowane jako narzędzie wspomagające, a nie jako rozwiązanie pierwszego wyboru. W praktyce oznacza to, że w przypadku problemów metabolicznych najpierw należy wykluczyć choroby tarczycy, zaburzenia hormonalne, niedobory witaminowe oraz przewlekły stan zapalny, a dopiero później analizować potencjalne wsparcie eksperymentalne.
Reset mitochondrialny nie polega na gwałtownej ingerencji, lecz na stopniowej poprawie środowiska komórkowego, w którym mitochondria funkcjonują. W wielu przypadkach największy efekt przynosi redukcja masy ciała, poprawa wrażliwości insulinowej oraz ograniczenie przewlekłego stresu. W tym kontekście peptydy takie jak MOTS-c mogą być rozważane w badaniach nad zaburzeniami metabolicznymi, natomiast SS-31 pozostaje bardziej domeną badań klinicznych nad chorobami związanymi z uszkodzeniem mitochondrialnym.
Podsumowując, reset mitochondrialny to koncepcja opisująca poprawę funkcjonowania komórkowych elektrowni poprzez redukcję stresu oksydacyjnego, wsparcie biogenezy oraz poprawę środowiska metabolicznego. Peptydy, o których mówi się w tym kontekście, należą głównie do grupy peptydów mitochondrialnych oraz regulatorów metabolicznych, jednak ich zastosowanie pozostaje ograniczone i w dużej mierze eksperymentalne. Najważniejsze pozostaje zrozumienie, że mitochondria reagują przede wszystkim na styl życia, a nie na pojedynczą substancję, dlatego każda decyzja o sięgnięciu po zaawansowane środki powinna być poprzedzona analizą korzyści i ryzyka oraz konsultacją ze specjalistą.
Jeżeli chcesz, mogę przygotować osobne opracowanie porównujące reset mitochondrialny poprzez styl życia z podejściem farmakologicznym, aby pokazać, gdzie leży realna różnica w bezpieczeństwie i skuteczności.
Bibliografia z hiperłączami
Lee C., Zeng J., Drew B.G., Sallam T., Martin-Montalvo A., Wan J., Kim S.J., Mehta H., Hevener A.L., de Cabo R., Cohen P. (2015). The mitochondrial-derived peptide MOTS-c promotes metabolic homeostasis and reduces obesity and insulin resistance. Cell Metabolism, 21(3), 443–454.
https://doi.org/10.1016/j.cmet.2015.02.009
Kim K.H., Son J.M., Benayoun B.A., Lee C. (2018). The mitochondrial-encoded peptide MOTS-c translocates to the nucleus to regulate nuclear gene expression in response to metabolic stress. Cell Metabolism, 28(3), 516–524.
https://doi.org/10.1016/j.cmet.2018.06.008
Szeto H.H. (2014). First-in-class cardiolipin-protective compound as a therapeutic agent to restore mitochondrial bioenergetics. British Journal of Pharmacology, 171(8), 2029–2050.
https://doi.org/10.1111/bph.12461
Birk A.V., Liu S., Soong Y., Mills W., Singh P., Warren J.D., Seshan S.V., Pardee J.D., Szeto H.H. (2013). The mitochondrial-targeted peptide SS-31 re-energizes ischemic mitochondria by interacting with cardiolipin. Journal of the American Society of Nephrology, 24(8), 1250–1261.
https://doi.org/10.1681/ASN.2012121216
Hood D.A., Memme J.M., Oliveira A.N., Triolo M. (2019). Maintenance of skeletal muscle mitochondria in health, exercise, and aging. Annual Review of Physiology, 81, 19–41.
https://doi.org/10.1146/annurev-physiol-020518-114310
Wu Z., Puigserver P., Andersson U., Zhang C., Adelmant G., Mootha V., Troy A., Cinti S., Lowell B., Scarpulla R.C., Spiegelman B.M. (1999). Mechanisms controlling mitochondrial biogenesis and respiration through the thermogenic coactivator PGC-1. Cell, 98(1), 115–124.
https://doi.org/10.1016/S0092-8674(00)80611-X
Cartee G.D., Hepple R.T., Bamman M.M., Zierath J.R. (2016). Exercise promotes healthy aging of skeletal muscle. Cell Metabolism, 23(6), 1034–1047.
https://doi.org/10.1016/j.cmet.2016.05.007
Wallace D.C. (2005). A mitochondrial paradigm of metabolic and degenerative diseases, aging, and cancer. Annual Review of Genetics, 39, 359–407.
https://doi.org/10.1146/annurev.genet.39.110304.095751
Picard M., Wallace D.C., Burelle Y. (2016). The rise of mitochondria in medicine. Mitochondrion, 30, 105–116.
https://doi.org/10.1016/j.mito.2016.07.003
Sikiric P., Seiwerth S., Rucman R., Turkovic B., Rokotov D.S., Brcic L., Sever M., Klicek R., Radic B., Drmic D., et al. (2010). Stable gastric pentadecapeptide BPC-157: novel therapy in gastrointestinal tract and beyond. Current Pharmaceutical Design, 16(10), 1224–1234.
https://doi.org/10.2174/138161210790965065
Clayton D.A. (1991). Replication and transcription of vertebrate mitochondrial DNA. Annual Review of Cell Biology, 7, 453–478.
https://doi.org/10.1146/annurev.cb.07.110191.002321
Spinazzi M., Casarin A., Pertegato V., Salviati L., Angelini C. (2012). Assessment of mitochondrial respiratory chain enzymatic activities on tissues and cultured cells. Nature Protocols, 7(6), 1235–1246.
https://doi.org/10.1038/nprot.2012.058
Dodaj komentarz